Česká a slovenská psychiatrie

Časopis
Psychiatrické společnosti ČLS JEP
a Psychiatrickej spoločnosti SLS
souborný článek / review article
KOMU A JAKÉ ANTIDEPRESIVUM
WHICH ANTIDEPRESSANT FOR WHOM?
Eva Čéšková
Psychiatrická klinika LF MU a FN Brno
Finanční podpora Výzkumným záměrem MSM0021622404
SOUHRN
Čéšková E. Komu a jaké antidepresivum
Faktory ovlivňující volbu léčby lze rozdělit na faktory související s léčbou a faktory související s nemocným. Při farmakoterapii deprese je nutné vzít v úvahu účinnost, snášenlivost a bezpečnost dostupných antidepresiv. Pro volbu antidepresiva u konkrétního nemocného je rozhodující klinický obraz deprese, tělesný stav nemocného (hlavně tělesná komorbidita), předchozí zkušenost s léčbou deprese, adherence k léčbě, individuální snášenlivost, preference a reaktivita na léčbu. Lékař musí spoléhat hlavně na pečlivou anamnézu. Jiný nástroj než observaci a klinické interview pro diagnostiku a volbu léčebné strategie v současné době v klinické praxi nemáme. V budoucnosti budeme mít nepochybně k dispozici objektivní ukazatele pro volbu léčby a sledování její účinnosti.
Klíčová slova: volba antidepresiva, účinnost, snášenlivost, bezpečnosti, klinický obraz, tělesná komorbidita, adherence, reaktivita na léčbu.
SUMMARY
Čéšková E. Which antidepressant for whom?
Factors influencing the treatment choice can be divided into factors related to treatment and factors related to patient. With pharmacotherapy it is necessary to take into consideration the efficacy, tolerability and safety of available antidepressants. Clinical picture of depression, adherence to the treatment, individual tolerability, preference and treatment reactivity are very important for the choice in individual patient. The doctor has to rely on the careful patients history. In the everyday clinical practice there is no other instrument than observation and clinical interview for diagnosing and choosing treatment strategy. In the future we will have undoubtedly objective indicators for the treatment choice and monitoring.
Key words: choice of antidepressants, efficacy, tolerability, safety, clinical picture, somatic comorbidity, adherence, treatment reactivity.
Při volbě antidepresiva (AD) je rozhodující lékař - jeho zkušenosti a znalosti o nemoci a léčbě - a nemocný - jeho aktuální psychický a tělesný stav, informovanost, zkušenost, preference. Pro zjednodušení lze faktory ovlivňující volbu rozdělit na faktory související s léčbou a související s nemocným.9
FAKTORY SOUVISEJÍCÍ S LÉČBOU
U každé léčby je nutné vzít v úvahu její účinnost, snášenlivost a bezpečnost.
ÚČINNOST AD
Cílem akutní antidepresivní léčby je dosažení remise. I když v průměru se účinnost jednotlivých AD významně neliší, lze najít rozdíly u některých subpopulací nemocných. Závažné deprese lépe reagují na AD se širším mechanismem účinku (duálně působící AD). Nedávno byla publikována metaanalýza randomizovaných klinických studií, které srovnávaly minimálně dvě AD ze skupiny tricyklických antidepresiv (TCA), specifických inhibitorů zpětného vychytávání serotoninu (SSRI) a inhibitorů zpětného vychytávání serotoninu a noradrenalinu (SNRI), trvajících minimálně 6 týdnů, v léčbě depresivní poruchy27 Celkem bylo analyzováno 15 studií, bylo zahrnuto 2458 léčených. Nejčastěji bylo dosaženo remise při léčbě SNRI (49% léčených), následovala TCA (44,1%) a SS-RI (37,7%). SNRI byla signifikantně účinnější než TCA (p > 0,05) a TCA a SNRI účinnější než SSRI (p > 0,001). Při léčbě SNRI bylo dosaženo vyššího procenta remisí u hospitalizovaných než u ambulantních nemocných. Je také známo, že ženy v premenopauze a děti lépe reagují na SSRI než na TCA.39, 40,17 Pokud je u dětí nebo mladistvých se středně těžkou až těžkou depresí ordinováno AD, měl by být použit fluoxetin, který v klinických studiích prokázal převahu prospěchu nad riziky léčby (včetně potenciálního rizika zhoršení sebevražedných myšlenek a chování) a byl pro tuto indikaci registrován i v ČR.17
Snášenlivost
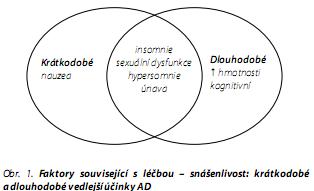
V poslední době se u řady nemocných klade důraz na dlouhodobou léčbu a tím se přesouvá pozornost k vedlejším účinkům, které přetrvávají po akutní léčbě (obr. 1). I některé vedlejší příznaky dříve považované za přechodné mohou přetrvávat. Detailně se této problematice věnoval Papakostas.33 Uvedl výsledky studie cílené na SSRI, dle které během prvních 2 týdnů byla pozorována nauzea u 82 % léčených, za 3 měsíce pouze u 32 %. Na rozdíl od toho procento léčených, kteří si stěžovali na zvýšení hmotnosti, se zvýšilo z 29 na 59 %. Insomnie, ospalost a sexuální dysfunkce se objevily brzo po zahájení léčby a přetrvávaly (64, 69 a 56 % léčených, po 3 měsících 69, 62 a 83 %).25 Vedlejší účinky jsou častou příčinou nonadherence. V naturalistické studii vysadilo po 4 měsících 51,2% léčených a % udávaly jako důvod vedlejší účinky26 Hu ve své práci uvedl sestupné pořadí vedlejších účinků, které léčené nejvíce obtěžovaly: sexuální dysfunkce (16,7%), ospalost a únava (16,5%), přírůstek hmotnosti (11,5%), insomnie (11,2%) a nauzea (5,7%).25 Insomnie, somnolence a únava se vyskytují přibližně ve stejné míře u SSRI a SNRI (venlafaxinu a duloxetinu). Nejčastěji vede k somnolenci a únavě mirtazapin a trazodon. Dle Monteja-Gonzalese30 sexuální dysfunkce udávalo při přímém dotazu 58 % léčených; pokud lékaři spoléhali na spontánní údaje, byl výskyt pouze 14 %. Dle Claytona11 byl nejnižší výskyt sexuální dysfunkce pozorován po bupropionu (28 %), při léčbě dalšími AD se pohyboval od 36 do 43 %.
Přírůstek hmotnosti
Výsledky velké průřezové studie, založené na elektronické databázi nemocných léčených pro unipolární depresi po dobu jednoho roku, udávaly přírůstek hmotnosti vyšší než 7% původní hmotnosti u 26% léčených mirtazapinem; u SSRI a venlafaxinu se procento pohybovalo od 16 do 19 %. Při léčbě bupropionem a nefazodonem byl výskyt nejmenší, 12% léčených.33 Málo údajů je k dispozici z kontrolovaných studií. Ke kognitivním vedlejším účinkům patří problémy s motivací, bdělostí a pamětí a snížení energie a zájmu o dění kolem.21
SSRI jsou preferována u somaticky nemocných, vzhledem k tomu, že nejsou kardiotoxická, minimálně snižují frekvenci pulzu a zvyšují variabilitu srdeční frekvence.35
Neovlivňují negativně glukózovou homeostázu, dokonce mohou vést ke zlepšení neuroendokrinologických parametrů u diabetů. Nejvíce byl studován fluoxetin, u kterého bylo zjištěno, že zvyšuje citlivost k inzulínu a snižuje hyperglykémii; noradrenergní TCA mají nejčastěji opačný efekt. Ukazuje se, že také duální AD nenarušují glukózovou homeostázu a jsou účinná u diabetické neuropatie.29 Z uvedených důvodů jsou SSRI preferována i u deprese u řady neurologických onemocnění.
Léčba AD u somaticky nemocných je účinná, i když zatím není dostatek studií s novými AD. Pomocí Cochranova registru bylo identifikováno 18 randomizovaných studií, zabývajících se touto problematikou (n = 838). NNT ("numer needed to treat", tj. počet nemocných, které je nutno léčit, aby se projevil efekt srovnávaného AD) měl hodnotu 4, tj. stejnou jako u tělesně zdravých depresivních nemocných. Autoři konstatovali, že AD u somaticky nemocných s depresí jsou účinná, nejsou rozdíly mezi skupinami a jednotlivými léky, i když byl pozorován trend ve prospěch TCA oproti SSRI, ale při léčbě TCA bylo více dropoutů.23
BEZPEČNOST
Podávání AD v graviditě
Deprese je relativně častá, udává se, že 1/10 žen trpí depresí během gravidity nebo po porodu.16 S rozšířením indikací AD dochází k nárůstu jejich podávání v graviditě. V poslední dekádě se zvýšilo užití SSRI v graviditě 2x paralelně s nárůstem podávání SSRI u žen ve fertilním věku. Dle holandských autorů byla expozice SSRI na 1000 těhotných žen v r. 1996 12,5, vr. 2004 již 28,5.1 Byly publikovány údaje, ze kterých vyplývá, že podávání SSRI těhotným ženám není zcela bezpečné.
Podávání SSRI a TCA v graviditě může vést k nižšímu gestačnímu věku a nižší hmotnosti novorozence. Je zvýšené riziko předčasných porodů a spontánních abortů, je také zvýšené riziko porodních komplikací, respiratorního distresu a pulmonální hypertenze u novorozence.33,34,10,12 I když AD obecně včetně SSRI nejsou považována za teratogenní, ukazuje se, že paroxetin je spojen se zvýšeným rizikem výskytu kongenitálních kardiálních abnormit.43
SSRI a riziko krvácení
Byla publikována řada kazuistik převážně o krvácení do gastrointestinálního traktu při podávání SSRI. Riziko zvyšuje kombinace SSRI s warfarinem, heparinem, nesteroidním protizánětlivými látkami a acylpyrinem.44,45
Syndrom z vysazení
Syndrom z vysazení byl popsán hlavně po SSRI, což je v kontextu s tím, jak jsou SSRI často užívána, a také po venlafaxinu. Je charakterizován závratěmi, ataxií, gastrointestinálními příznaky, chřipkovými příznaky a parestéziemi.2
Lékové interakce
S podáváním některých AD, zvláště SSRI, je spojeno riziko lékových interakcí. Je to dáno tím, že SSRI jsou nejen metabolizována enzymatickým systémem CYP 450, ale také ho inhibují; tedy při podávání SSRI se z nemocných stávají pomalí metabolizátoři. Tento fakt je klinicky významný pouze u velmi malého počtu léčených, zvláště v případě polyfarmacie. Některá novější AD, např. milnacipran a desvenlafaxin, který je ve stadiu klinického zkoušení, nejsou metabolizována enzymatickým systémem CYP 450 a minimálně ho inhibují. Tato AD jsou spojena s nižším rizikem lékových interakcí, což je výhodné u depresivních nemocných s vysokou tělesnou komorbiditou a polyfarmacií.8,9,15
Otázka snášenlivosti a bezpečnosti hraje velkou roli v léčbě deprese u seniorů. Ve vyšší věkové kategorii je deprese častá a koreluje s horším funkčním stavem a kvalitou života. Při volbě AD bychom měli kromě přítomných somatických onemocnění a jejich léčby zohlednit sníženou kapacitu biodegradace a změny neuroplasticity transmiterových systémů stárnoucího mozku.24,38
FAKTORY SOUVISEJÍCÍ S NEMOCNÝM
K faktorům souvisejícím s nemocným patří 1. psychický stav (klinický obraz), 2. tělesný stav (komorbidita), 3. předchozí zkušenost a adherence, 4. individuální snášenlivost, preference a reaktivita na léčbu.
Klinický obraz
Pro volbu AD dle převažujících příznaků chybějí kontrolované studie, přesto v praxi takto postupujeme. U útlumové klinické formy deprese jsou preferovány inhibitory zpětného vychytávání dopaminu a noradrenalinu (DNRI), z těchto je u nás jediný dostupný zástupce bupropion ve formě s pozvolným uvolňováním (f o. Welbutrin). U úzkostné formy upřednostňujeme antagonisty serotoninu a inhibitory zpětného vychytávání serotoninu (SARI) s jeho zástupce trazodonem, který je opět u nás dostupný pouze ve formě s pozvolným uvolňováním (f. o. Trittico AC) a noradrenergní a specifická serotonergní AD (NaSSA); z této skupiny je k dispozici mirtazapin, který je již vyráběn několika generickými firmami. U nevyhraněné formy lze použít SSRI, konkrétně citalopram a sertralin, které mají relativně nejvyrovnanější efekt na útlum a úzkost a specifické inhibitory zpětného vychytávání serotoninu a noradrenalinu (SNRI). Z této skupiny je dostupný venlafaxin, vyráběný již řadou generických firem, a milnacipran (f. o. Ixel). Tento postup spočívá na zjednodušené představě, že porucha (deficit) jednotlivých základních neurotransmiterů je spojena s výskytem určitých příznaků.37,18,7 Tomuto přístupu se dostalo nepřímé podpory současným pohledem na depresivní poruchu. Jednotlivé depresivní příznaky jsou spojovány s dysfunkcí určitých oblastí CNS a neuronálních drah, spojených s jednotlivými neurotransmitery (hlavně serotoninu, noradrenalinu a dopaminu), které jsou ve vzájemné interakci. Depresivní nálada nejspíše souvisí se zvýšenou aktivací prefrontálního limbického kortexu, snížení zájmu a hedonie se sníženou stimulací hypotalamu (serotonin a noradrenalin) nebo limbické oblasti (nucleus accumbens - dopamin), úzkost s abnormní stimulací amygdal (serotonin, noradrenalin), psychomotorická agitovanost nebo útlum s abnormní aktivací nukleus kaudatus (serotonin, noradrenalin) a mozečku (noradrenalin). Dle současného pohledu je depresivní syndrom systémová porucha, dysregulace neuronální sítě, podmíněná kognitivním, emočním nebo somatickým stresem, konzistentně zahrnující limbické a kortikální oblasti a replikovatelné změny navozené různými způsoby antidepresivní léčby.28
Tělesný stav - komorbidita
Vedoucí příčinou mortality obecně je nepochybně kardiovaskulární onemocnění, proto i tato problematika byla nejvíce studována a je v popředí zájmu. Před více než 20 lety byla identifikována deprese jako rizikový faktor pro kardiální události u nemocných s koronárni chorobou srdeční5 a před 15 lety bylo zjištěno, že zvyšuje riziko mortality po akutním infarktu myokardu.22 Protože deprese je léčitelná a představuje modifikovatelný faktor, byla vyslovena domněnka, že léčba deprese by mohla zlepšit prognózu u depresivních nemocných s koronárni chorobou. Výsledky zatím nejsou konzistentní, i když poslední metaanalýzy podporují předpoklad, že deprese je nezávislý rizikový faktor pro kardiovaskulární morbiditu a mortalitu u pacientů s koronárni chorobou.4,41
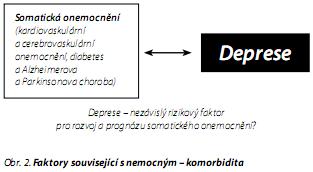
Pro depresivního nemocného se somatickým onemocněním je nejdůležitější otázka, jak antidepresivní léčba ovlivní jeho tělesnou chorobu a její průběh. Sníží léčba deprese riziko kardiálních událostí po infarktu myokardu? Na tuto otázku se snažily odpovědět pouze dvě studie (the Enhancing Recovery in Coronary Heart Disease - ENRICHED a the Myocardial Infarction and Depression Intervention Trial - MIND-IT), které ukázaly, že intervence mají malý vliv na přežití,3,42 a v další analýze obou studií byla zjištěna nižší incidence kardiálních událostí u responderů na antidepresivní léčbu.6,13
Další možnost nabízí farmakogenetika. Bylo zjištěno, že pacienti se stabilní srdeční angínou a krátkou alelou serotoninového transportéru jsou častěji depresivní, mají vyšší úroveň stresu a vyšší exkreci noradrenalinu a také vyšší výskyt deprese a kardiálních událostí.31
Neméně důležitý je fakt, že deprese může být nezávislým rizikovým faktorem pro řadu somatických onemocnění19 (obr. 2).
Předchozí zkušenost a adherence
Pro jedince je velmi důležité, zda opětné nasazení již dříve úspěšné léčby bude opět úspěšné. Kontrolované studie ukazují úspěšnost u 2/3 nemocných; remitéři reagují lépe než nemocní, kteří před vysazením léčby reagovali pouze částečně.20
Někdy je popisována tzv. tachyfylaxe (léková tolerance, pop-out fenomén), kdy po určité době u léčených SSRI může dojít ke stavu apatie, snížené motivace a snížené afektivní reaktivitě. Tento fenomén může být teoreticky dán významným zvýšením serotoninové aktivity v mozku, které může vést ke kompenzatornímu snížení noradrenalinu a dopaminu. Toto lze zvládnout změnou na SNRI nebo přídatnou léčbou noradrenergními a dopaminergními látkami k SSRI.39
Pokud má nemocný ve své anamnéze nonadherenci, je namístě velmi pečlivé stanovení důvodů vysazení (vedlejší účinky mohou být důvodem až u % léčených, komorbidita se závislostí, špatná komunikace mezi lékařem a pacientem), z nichž řadě je možné předejít a jsou ovlivnitelné.46
Individuální snášenlivost, preference a reaktivita na léčbu
Individuální snášenlivost nepochybně do určité míry souvisí s metabolismem jedince. Tento předpoklad podporují výsledky studie, která zjistila, že ve skupině nemocných léčených venlafaxinem měli pomalí metabolizátoři ve srovnání s rychlými metabolizátory více vedlejších účinků. Rozdíly v léčebném efektu nebyly signifikantní.36
Kromě toho, že nemocný by měl sdělit lékaři, které vedlejší účinky jsou pro něj snesitelné a nepodstatné a které nelze tolerovat, se dnes nabízí možnost snášenlivost a perspektivně i reaktivitu na léčbu predikovat.
Farmakogenetika vstoupila do klinické psychiatrické praxe se schválením FDA testu AmpliChip450. Tento stanoví genotypy dvou cytochromů P450 2D6 (CYP2D6) a 2C19(CYP2C19). CYP2D6 je důležitý pro metabolismus řady AD a antipsychotik, CYP2C19 pro metabolismus některých AD. Touto problematikou se detailněji zabývá brněnská psychiatrická klinika.47 Současná moderní AD mají nízkou toxicitu, takže zpomalení jejich metabolismu není významně klinicky relevantní, proto rutinní genetické testování CYP2D6 u každého jedince před zahájením léčby není považováno za nutné. Informace o aktivitě CY-P2D6 může být důležitým vodítkem pro klinickou praxi, pokud je nemocný léčen inhibitory CYP2D6 a má výrazné vedlejší účinky (mohlo by se jednat o pomalého metabolizátora a bylo by vhodné snížit dávky AD nebo zvolit AD, které se nemetab olizuj e pomocí CYP2D6) nebo při dobré adherenci nereaguje na léčbu (mohlo by se jednat o ultrarychlé metabolizátory a bylo by třeba zvýšit dávku AD) a při plánované kombinaci několika inhibitorů CYP2D6. Tato kombinace není obecně doporučována, protože je považována za rizikovou. V případě pomalých metabolizátorů by bylo riziko velmi vysoké, naopak ultra-rychlý metabolizátor by mohl z léčby profitovat - došlo by k úpravě fenotypu do pásma normy.14,47
ZÁVĚR
Pro zlepšení antidepresivní léčby je nutné překlenout mezeru mezi výzkumem a klinickou praxí. I v běžné praxi je nutné pečlivé monitorování účinnosti zvolené antidepresivní léčby. Globální hodnocení účinnosti nebývá dostačující, protože mohou uniknout reziduálni příznaky a počínající relaps či recidíva. Je nutné se ptát cíleně na příznaky, které jsou relevantní pro depresivní poruchu, adherenci, vedlejší účinky a fungování nemocného. Jiný nástroj než observaci a klinické interview v současné době v klinické praxi nemáme. V blízké budoucnosti bude zřejmě možná volba léčby na bázi objektivního hodnocení funkce mozku v kontextu známých rizikových faktorů (genetických, somatických, psychosociálních).
LITERATURA
- 1. Bakker MK, Rolling P, Van den Berg PB et al. Increase in use of selective serotonin reuptake inhibitors in pregnancy during the last decade, a population-based cohort study from The Netherlands. Br J Clin Pharmacol 2008; 65: 600-606.
- 2. Baldwin DS, Montgomery SA, Nil R, Lader M. Discontinuation symptoms in depression and anxiety disorder. Int J Neuropsychopharmacol 2007; 10: 73-84.
- 3. Bergman LF, Blumenthal J, Burg M et al. Effects of treating depression and low perceived social support on clinical events after myocardial infarction: the Enhancing recovery in coronary heart disease patients (ENRICHED). Randomized trial. JAMA 2003; 289: 3106-3116.
- 4. Barth J, Schumacher M, Hermann-Lingen C. Depression as a risk factor for mortality in patients with coronary heart disease: a meta-analysis. Psychosom Med 2004; 66: 802-813.
- 5. Carney RM, Rich MW, Freedland KE et al. Major depressive disorder predicts cardiac events in patients with coronary artery disease. Psychosom Med 1988; 50: 627-633.
- 6. Carney RM, Blumenthal JA, Freedlan KE et al. Depression and late mortality after myocardial infarction in the Enhancing recovery in coronary heart disease (ENRICHED) study. Psychosom Med 2004; 66: 466-474.
- 7. Čéšková E. Možnosti farmakoterapie deprese. Psychiat pro Praxi 2005; 6: 233-236.
- 8. Čéšková E. Duálně působící antidepresiva. Remedia 2006; 16: 594-597.
- 9. Čéšková E. Jak správně zvolit antidepresivum. Psychiat pro Praxi 2007; 8: 229-231.
- 10. Chambers CD, Hernande-Diaz S, Van Marter LJ et al. Selective serotonin-reuptake inhibitors and risk of persistent pulmonary hypertension of the newborn. N Engl J Med 2006; 354: 579-587.
- 11. Clayton AH, Pradko JF, Drift HA et al. Prevalence of sexual dysfunction among newer antidepressants. J Clin Psychiatry 2002; 63: 357-366.
- 12. Davis RL, Rubanowice D, McPhillips H et al. HMO Research Network Center for Education, Research in Therapeutics. Risk of congenital malformations, and perinatal events among infants exposed to antidepressant medications during pregnancy. Pharmacoepidemiol Drug Saf 2007; 16: 1086-1094.
- 13. De Jonge P, Honig A, Van Melie JP et al. Nonresponse to treatment for depression following myocardial infarction. Association with subsequent cardiac events. Am J Psychiatry 2007; 164: 1371-1378.
- 14. De Leon J, Armstrong SC, Cozza KL. Clinical guidelines for psychiatrists for the use of pharmacogenetic treating for CYP450 2D6 and CYP450 2C19. Psychosomatics 2006; 47: 75-85.
- 15. De Martinis N, Yeung PP, Entsuah R, Manleym AL. A double-blind, placebo-controlled study of the efficacy and safety of desvenlafaxine succinate in the treatment of major depressive disorder. J Clin Psychiatry 2007; 68: 677-688.
- 16. Diez PM, Williams SB, Callaghan WM et al. Clinically identified maternal depression before, during, and after pregnancies ending in live births. Am J Psychiatry 2007; 164: 1515-1520.
- 17. Drtílková L Klinická vodítka NICE léčby depresivních poruch u dětí a adolescentů. Psychiat pro Praxi 2007; 4: 158-161.
- 18. Dunlop BW, Nemeroff CB. The role of dopamine in the pathophysiology of depression. Arch Gen Psychiatry 2007; 64: 327-337.
- 19. Evans DL, Charney DS, Lewis L et al. Mood disorders in the medically ill: scientific review and recommendations. Biol Psychiatry 2005; 58: 175-189.
- 20. Fava M, Schmidt ME, Zhang S et al. Treatment approaches to major depressive disorder relapse, part 2: reinitiation of antidepressant treatment. Psychother Psychosom 2002; 71: 195-199.
- 21. Fava M, Graves LM, Benazzi F et al. A cross-sectional study of the prevalence of cognitive and physical symptoms during long-term antidepressant treatment. J Clin Psychiatry 2006; 67: 1754-1759.
- 22. Frasure-Smith N, Lesperance R, Takajíc M. Depression following myocardial infarction: impact on 6-months survival. JAMA 1993; 270: 1819-1825.
- 23. Gill D, Hatcher S. Antidepressants for depression in medical illness. Cochrane Database Syst Rev 2007; 18: CD001312.
- 24. Holmerová I, Vaňková H, Dragomirecká E et al. Depresivní syndrom u seniorů, významný a dosud nedoceněný problém. Psychiatr pro Praxi 2006; 4: 182-184.
- 25. Hu XH, Bull SA, Hunkeler EM et al. Incidence and duration of side effects and those rated as bothersome with selective serotonin reuptake inhibitor treatment for depression: patient report versus physician estimate. J Clin Psychiatry 2004; 65: 959-965.
- 26. Lin EH, Von Korff M, Lin E et al. The role of the primary care physician in patients adherence to antidepressant therapy. Med Care 1995; 33: 67-74.
- 27. Machado M, Iskedjian M, Ruin I, Einarson TR. Remission, dropouts, and adverse drug reaction rates in major depressive disorder. A meta-analysis of head-to-head trials. Curr Med Res Opin2006;22: 1825-1837.
- 28. Mayberg HS. Defining the neural circuitry of depression: toward a new nosology with therapeutic implications. Biol Psychiatry 2007; 61: 729-730.
- 29. Mclntyre RS, Soczynska J, Konarski JZ et al. The effect of antidepressants on glucose homeostasis and insulin sensitivity: synthesis and mechanisms. Ex-per Opin Drug Saf 2006; 5: 157-168.
- 30. Montejo-Gonzales AL, Llorca G, Izquierdo JA et al. SSRI-induced sexual dysfunction: fluoxetine, paroxetine, sertraline, and fluvoxamine in a prospective, multicenter, and descriptive clinical study of 344 patients. J Sex Marit Ther 1997; 23: 176-194.
- 31. Nakatani D, Sato H, Sakata Y et al. Influence of serotonin transporter gene polymorphism on depressive symptoms and new cardiac events after acute myocardial infarction. Am Heart J 2005; 150: 652-658.
- 32. Oberlander TF, Warburton W, Misri S et al. Neonatal outcomes after prenatal exposure to selective serotonin reuptake inhibitor antidepressants and maternal depression using population-based linked health data. Arch Gen Psychiatry 2006; 63: 898-906.
- 33. Papakostas GI. Limitations of contemporary antidepressants: tolerability J Clin Psychiatry 2007; 68 (suppl. 10): 11-17.
- 34. Rahimi R, Nikfar S, Abdollahi M. Pregnancy outcomes following exposure to serotonin reuptake inhibitors: a meta-analysis of clinical trials. Reprod Toxicol 2006; 22: 571-575.
- 35. Roose SR Treatment of depression in patients with heart disease. Biol Psychiatry 2003; 54: 262-268.
- 36. Shams ME, Arneth B, Hiemke C et al. CYP2D6 polymorphism and clinical effect of the antidepressant venlafaxine. J Clin Pharm Ther 2006; 31: 493-502.
- 37. Stahl SM. Essentials psychopharmacology 2nd ed. Cambridge: Cambridge University Press; 2000.
- 38. Sulcová A. Stárnoucí mozek a psychotropní látky Psychiatrie 2009; 13: 29-32.
- 39. Thase ME, Ninan PT. New goals in the treatment of depression: moving toward recovery. Psychopharmacol Bull 2002; 36 (suppl. 2): 24-35.
- 40. Thase M, Entsuahm R, Cantillon M, Kornstein SG. Relative antidepressant efficacy of venlafaxine and SSRIs: sex-age interactions. J Womens Health 2005; 14: 609-616.
- 41. Van Melle J, De Jonge P, Spijkerman TA et al. Prognostic association of depression following myocardial infarction with mortality and cardiovascular events: a meta-analysis. Psychosom Med 2004; 66: 814-822.
- 42. Van Melle J, De Jonge P, Honig A et al. Effects of antidepressant treatment following myocardial infarction. Br J Psychiatry 2007; 190: 460-466.
- 43. Way CM. Safety of newer antidepressants in pregnancy. Pharmacotherapy 2007; 27: 546-552.
- 44. Weinrieb RM, Auriacombe M, Lynch KG, Lewis JD. Selective serotonin re-uptake inhibitors and the risk of bleeding. Expert Opin Drug Saf 2005; 4: 337-344.
- 45. Wessinger S, Kaplan M, Choi L et al. Increased use of selective serotonin reuptake inhibitors in patients admitted with gastrointestinal haemorrhage: a multicentre retrospective analysis. Aliment Pharmacol Ther 2006; 23: 937-944.
- 46. Zajecka JM. Augmentation strategies to increase antidepressant tolerability. J Clin Psychiatry 2007; 68 (suppl. 10): 23-27.
- 47. Žourková A. Možnosti užití personalizované medicíny v léčbě depresivních poruch. Psychiatrie 2007; 11 (suppl. 2):104-106.





