Česká a slovenská psychiatrie

Časopis
Psychiatrické společnosti ČLS JEP
a Psychiatrickej spoločnosti SLS
souborný článek / review article
ZNÁME MECHANISMUS ÚČINKU ELEKTROKONVULZIVNÍ LÉČBY?
ARE WE FAMILIAR WITH THE MECHANISM OF ACTION OF ELECTROCONVULSIVE THERAPY?
Jakub Albrecht1, Lucie Kališová1, Tadeáš Mareš1, Kateřina Mádlová1, Jiří Michalec1, Markéta Kubínová1, Pavel Doubek1, Jiří Raboch1, Martin Anders1
1 Psychiatrická klinika 1. LF UK a VFN v Praze
Práce byla podpořena výzkumnými projekty: MZ VES 15-30439A, RVO VFN 64165, Q27/LF1.
SOUHRN
Albrecht J, Kališová L, Mareš T, Mádlová K, Michalec J, Kubínová M, Doubek P, Raboch J, Anders M. Známe mechanismus účinku elektrokonvulzivní léčby?
Elektrokonvulzivní terapie je během času osvědčenou, bezpečnou, účinnou a v mnoha případech nenahraditelnou léčbou širokého spektra neuropsychiatrických onemocnění, ale mechanismus účinku zůstává nadále nevysvětlený Byla publikována velká řada prací, které popisují dílčí změny po konvulzích u různých diagnóz, celkem více než sto hypotéz. Tento článek se snaží zmapovat soudobé poznatky a nastínit další vývoj.
Klíčová slova: EKT, elektrokonvulzivní léčba, indikace, mechanismus účinku, neuroneogeneze, neuroplasticita, zánět, katatonie, deprese, mánie, stupor
SUMMARY
Albrecht J, Kališová L, Mareš T, Mádlová K, Michalec J, Kubínová M, Doubek P, Raboch J, Anders M. Are we familiar with the mechanism of action of electroconvulsive therapy?
Electro convulsive therapy is a proven, safe, effective, and in many cases irreplaceable, treatment for a wide range of neu-ropsychiatric illnesses over time, but the mechanism of action remains unexplained. A large number of papers have been published that describe partial changes after convulsions in various diagnoses, more than a hundred hypotheses. This article attempts to map current knowledge and outline further developments.
Key words: ECT, electroconvulsive therapy, indications, mechanism of action, neuroneogenesis, neuroplasticity, inflamation, catatonia, depression, mania, stupor
ÚVOD
Na sklonku druhého decennia 21. století, po téměř sto letech používání, se zdá, že by mělo být k dispozici dostatečné množství informací o mechanismu účinku elektrokonvulzivní léčby (EKT), aby mohla existovat jednotná, opakovaně potvrzená teorie mechanismu účinku EKT u neuropsychiatrických onemocnění. Dosud nebyla publikována žádná, která by modelovala komplexitu účinku a současně vysvětlovala neobvyklou účinnost této nenahraditelné biologické modality efektivní v širokém spektru vážnějších neuropsychiatrických poruch.
Snad jedinečnost každého pacienta, diagnostických okruhů, jejich endofenotypů, genetického polymorfismu a různorodost etiopatogeneze vede ke komplikovanosti problému. EKT patří do základního armamentaria minimálně invazivních, konvulzivních metod v léčbě akutních a často život ohrožujících stavů; v několika indikacích pak ultimum refugium.
Bylo publikováno přes sto různých hypotéz (Sackeim, Brain Stimulation Congress, Barcelona 2017). V recentní české literatuře postrádáme přehled novějších hypotéz, nicméně si nedovolujeme téma zcela vyčerpat.
Pacienti se na mechanismus účinku budou stále častěji dotazovat, zvláště když se počet odkazů na "elektrokonvulzivní léčba" na Googlu pohybuje kolem 23 tisíc jen v českém jazyce a 840 tisíc anglicky měsíčně. Reklamní portál Google AdWords udává četnost za jeden měsíc vyhledávání sousloví "electroconvulsive therapy" v rozmezí 100 tisíc až jeden milion celosvětově, nejčastěji spolu s hesly: "léčba", "šok", jiné, "velká depresivní porucha" a "deprese" (v tomto pořadí). Počet článků na Web of Science ke klíčovému slovu "electroconvulsive therapy" dosáhl 7 782 ke dni 1. 9. 2017 a přibývají zde v průměru o 380 publikací ročně v posledních sedmi letech.
"To nikdo neví?" je nedostatečná odpověď! Účinek je "komplexní", nebo případně, že "mechanismus účinku neznáme, ale víme, že to prostě funguje", by neměly být dostatečnými odpověďmi. Mnoho biologických i psychologických teorií bylo vyvráceno. Jiné teorie jsou výběrové, určené pro specifické neurobiologické působení.
Ucelený, ale již letitý pohled nabízí monografie z roku 1993.1 Tento článek si klade za cíl přehlédnout zajímavé zdroje ve snaze kategorizovat poznatky, ne však (bohužel) předložit jednotnou funkční teorii.
PREHISTORIE A HISTORIE
Šokové metody léčby vycházely z toho, že šok měl vést k navození emocionální krize, po jejímž zvládnutí se očekávalo zlepšení psychického stavu pacienta. Traduje se, že jednou z prvních "šokových" metod byl ve staroindické Ajurvédě ukotvený postup, kdy melancholický pacient byl připoután ke kůlu, a proti němu se rozeběhnul cvičený slon, který na poslední chvíli (obvykle) změnil směr. Prožitek smrtelné úzkosti měl navrátit nemocnému ztracenou duševní rovnováhu.2 Účinek vyvolání celotělových křečí spojených s více či méně prolongovaným bezvědomím a amencí ovlivňující pozitivně duševní stav nemocných pacientů je empiricky i literárně podložen více než 2500 let.3
Experimentální konvulzivní léčba
Nověji zkoumanou konvulzivní ("šokovou") metodou je magnetokonvulzivní terapie (MST, magnetic seizure therapy),4 při níž je vyvolání epileptiformního paroxysmu způsobeno velmi silnou rázovou magnetickou indukcí a na rozdíl od repetitivní transkraniální magnetické stimulace (rTMS) je magnetická indukce až řádově vyšší. Fokální elektricky administrovaná záchvatová terapie (FEAST, Focally electrically administred seizure therapy),5,6 u níž působí "jednosměrný proud" (ze sinusovky střídavého proudu je zachována pouze vrcholová část), která podobně jako transkraniální stejnosměrná stimulace (tDCS) výrazně zdůrazňuje lokalizaci elektrod (odlišné změny pod anodou a katodou), dlí dosud v plenkách. Zajímavé jsou pilotní práce o využití kombinace rTMS a EKT.
Pak už jen v kuloárech se od roku 2002 mluví o transkraniální pulzní ultrazvukové modulaci (transcranial pulsed ultrasound modulation - TPUM; transcranial ultrasound stimulation - TUS), která vznikla v rámci amerického obranného výzkumu (DARPA) a využívá ultrazvuk nízké intenzity a nízké frekvence (low intensity, low frequency ultrasound, LILFU).7
PRINCIP ÚČINKU ELEKTROKONVULZIVNÍ TERAPIE
Malý exkurz k dvojjedinosti elektromagnetického pole
Dovolujeme si připomenout, že podstata jevů elektrických a magnetických byla nastíněna Ampérem, Voltem a Coloumbem a matematické principy byly ukotveny Ohmem v zákoně z r. 1827. Práce Öersteda, Faradaye a především Jamese Maxwella vedly ke vzniku teorie elektromagnetického pole až roku 1873. Pochopení podstaty elektroslabé interakce (sjednocené teorie slabé interakce a elektromagnetické síly) Winbergem, Salamem a Glashowem se datuje k roku 1967 a omlouváme se za odbočku ke standardnímu modelu částic kvantové mechaniky a kvantové teorii.
Výzkum působení silného magnetického pole s vyvoláním léčebného epileptiformního záchvatu v rámci magnetické záchvatové terapie ("magnetošoky") patří blízké budoucnosti, ale již s prokázaným antidepresivním efektem u rezistentního depresivního syndromu.8
Široké indikační spektrum EKT
Je známa účinnost v mnoha indikačních - diagnostických - okruzích, které nemají jednotnou anebo jednoznačnou etiopatogenezi:9
- rezistentní středně těžké až těžké depresivní epizody (velká depresivní porucha, organická depresivní porucha)10
- rezistentní depresivní fáze (bipolární afektivní porucha, schizoafektivní porucha)10
- rezistentní manické fáze (bipolární afektivní porucha, schizoafektivní porucha)11
- rezistentní smíšené fáze s psychotickými příznaky (bipolární afektivní porucha)11
- rezistentní psychózy (schizofrenie, organické psychotické poruchy)12
- těžké psychotické a afektivní stavy komplikované stuporem13
- katatonie14,15
- mania delirans16,17
- suicidální chování jinak neřešitelné18
- agitovaný, agresivní pacient nereagující na jinou léčbu (např. u syndromu demence)19
- neuroleptický maligní syndrom20
- status epilepticus21,22
- parkinsonismus s "on-off fenomény"23
- tardivní dyskinézy24
- delirium25
- na žádost pacienta v udržovací léčbě (c-EKT, continuation; m-EKT, maintenace;
r-EKT, rescue)26,27- při selhání psychofarmakologické léčby a dalších postupů - ultimum refugium.
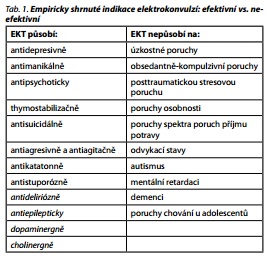
Oblasti minimálního nebo neprokázaného účinku
Nebyla prokázána dostatečná efektivita u úzkostných poruch, obsedantně-kompulzivní poruchy, posttraumatické stresové poruchy,28 poruch osobnosti, spektra poruch příjmu potravy, syndromu závislosti a u odvykacích stavů, autismu, mentální retardace a demence.
Jsou však ojediněle publikovány jednotlivé kazuistiky, kdy i u některých pacientů z uvedených diagnostických oblastí došlo vlivem EKT ke zlepšení stavu.29
Krátká poznámka k rezistenci
Již samotná snaha o definici rezistence k léčbě naráží na silnou odolnost. Jen okolo 33 % zachycených depresivních pacientů má adekvátní léčbu.30 Na stole je též hypotéza příznaku rozvoje neurodegenerativního onemocnění (validní a jednoduchý diagnostický/klinický nástroj dosud chybí). Jak potom definovat úzdravu: jako klinickou remisi ("klinická normoforie"), či snížení vnímavosti (emoční oploštění, bublina, skleník etc.), úplné funkční zotavení (návrat funkční schopnosti, beze změn osobnosti a kognice), syndromologickou úzdravu (nenaplňování kritérií), nebo jako absenci negativních a přítomnost pozitivních afektů (euforie)?
Výhody a nevýhody EKT
Mezi nezpochybnitelné přednosti EKT patří: rychlý nástup účinku (po 3-4 aplikacích viditelný klinický efekt); neobvyklá účinnost (responze u bezmála 90 % k léčbě rezistentních depresivních stavů); vysoká bezpečnost (mortalita jen 2,1 na 100 000 výkonů dle recentní meta-analýzy 766 180 aplikací z 32 zemí z 201731); minimum komplikací (přechodné postižení kognitivních funkcí, jen asi v 7-10% delirium - zde je otázka vlivu anestetika a hypoxie).
Porucha kognitivních funkcí jako hlavní nežádoucí účinek je v 98 % plně reverzibilní32 do 6 měsíců, u drtivé většiny pacientů do 6 týdnů zjistitelná jen specializovanými neuropsychologickými testy. EKT nepůsobí negativně na morfologii mozku (nevzniká "jizva", přestože ovlivňuje zánětlivé mechanismy). EKT nepůsobí trvalé změny osobnosti (viz program CIA MkUltra v 50. letech 20. století v USA). EKT působí amnézii na výkon samotný (krátká anterográdní i retrográdní amnézie).
Mezi nevýhody lze uvést: společenskou stigmatizaci33 (pohled "filmového konzumenta", např. Formanův Přelet nad kukaččím hnízdem nebo Rekviem za sen a jiné); domněnky o mučících a středověkých metodách; názory ohledně trestání duševně nemocných; veřejnost, zejm. nejbližší nemocných se domnívá, že se jedná o obsolentní metodu vyhrazenou pro "největší blázny", která "gumuje mozek" a "mění osobnost".
MECHANISMUS ÚČINKU ELEKTROKONVULZIVNÍ TERAPIE
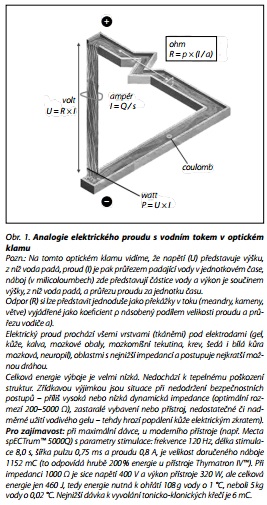
V zásadě se jedná o vyvolání generalizovaného epileptiformního paroxysmu působením elektrické energie (obr. 1).
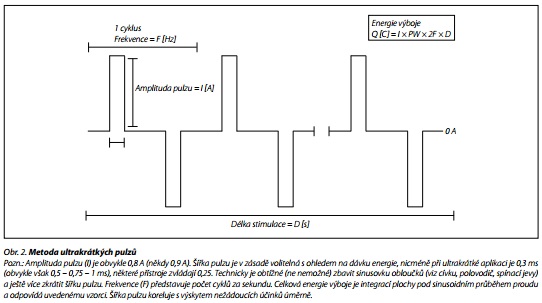
Elektrický proud je střídavý, s nulovou střední hodnotou, modulovaný do obdélníkových pulzů s (ideálně) ultrakrátkou (ultrabrief pulse; 0,25 - 0,3 - 0, 5 ms) nebo "klasicky" krátkou základnou (brief pulse; 0,5 - 0,75 -1 ms), obr. 2.
Tento proud nemá přímé elektrochemické účinky - nepůsobí elektrolýzu - periodicky se střídá (podle frekvence: 20-120 Hz) polarita: katoda (záporná elektroda) se mění s anodou (kladná elektroda) a nabité částice nikam fakticky neputují.
Zapojení skalpových elektrod je standardně bitemporální, bifrontální nebo unilaterální nad nedominantní hemisférou (detailnější pohled viz34).
Pro bezpečný průběh musí být zajištěna co nejnižší dynamická impedance (zjednodušeně odpor střídavého proudu přímo při jeho průchodu vodičem), k čemuž slouží mimo jiné abrazivní či elektrovodivé gely a další opatření.35
Principy účinnosti a bezpečnosti EKT
Ve smyslu indukce epileptiformního záchvatu je místem, odkud se záchvat sekundárně šíří, hippocampus, ať už se jedná o "chemické", nebo "elektrické šoky". Záchvat externě vyvolaný, ať tak, či onak, je primárně fokální a sekundárně generalizovaný (locus minoris resistetiae).
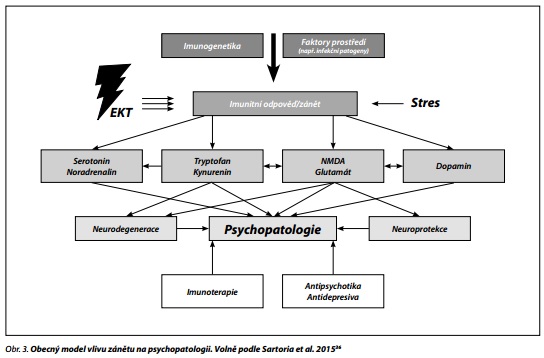
Účinky jsou jak morfologické (ve smyslu quo ad bonům - viz níže vliv na neuroneogenezi a neuroplasticitu - nejsou prokázány destruktivní změny nebo atrofie šedé kůry, ba naopak), tak biochemické, ale i funkční, jsou i důkazy pro přímé působení na genetickou expresi, dochází ke změnám klidových potenciálů (dlouhodobá potenciace a deprese), mění se parametry subklinického zánětu doprovázejícího psychiatrická onemocnění mozku (obr. 3).
Účinek je odvislý od dávky, která je charakterizovaná energií výboje (zde hraje roli frekvence, šířka pulzu, amplituda pulzu a délka stimulace), volbou titrace dávky výboje a dalšími parametry (četnost v týdnu, celková kumulativní dávka, neabruptivní ukončení aplikace, přechod na udržovací léčbu atp.).
Titrace energie má význam vzhledem k uvedeným měnitelným parametrům daného výboje a z toho plynoucích implikací pro klinickou praxi.37
Korelace mezi dávkou a účinností je dána hlavně adekvátním elektroencefalografickým záznamem paroxysmu (délka iktální aktivity, míra suprese a eventuálně spektrální analýza), který (zjednodušeně řečeno) má představovat 20 - 60 s iktální aktivity typu grand mal s úplným návratem do theta, resp. delta aktivity. Nežádoucí účinky jsou (i z pohledu mechanismu účinku) rovněž rozhodující pro bezpečnost, účinnost a snášenlivost, a byť jsou v drtivé většině případů mírné a zcela reverzibilní, ukazuje se, že parametry, které jsou sledovatelné jak klinicky (např. sledování "time to recovery", tedy doby do nabytí plné orientace - u obsolentních zařízení bývala tato doba v řádu desítek hodin, nyní cca 3 - 12 minut), tak neuropsychiatrickými testovými bateriemi, mohou spoluvysvětlovat mechanismus účinku (zejména působení na hippokampální formaci).
Dávka energie je ideálně dodána moderním přístrojem s důrazem na bezpečnost pacienta a precizní volbou jednotlivých stimulačních parametrů. Správná volba parametrů, stejně jako sledování klinického průběhu (čas do zotavení, kognitivní výkonnost v průběhu léčby, sledování deliriózních příznaků a jejich eliminace např. změnou anestetika) a elektroencefalografického korelátu (z obou hemisfér) vede jednoznačně k minimalizaci rizik, a to především kognitivních nežádoucích účinků.
Další čerstvé poznatky o možnostech zvýšení účinnosti, titraci energie podle konvulzivního prahu, monitorování EEG, komedikaci při augmentační strategii, volbě anestetika, zvýšení bezpečnosti pro pacienta a další zásadní minimalizaci nežádoucích účinků jsou nad rámec tohoto sdělení. Dovolujeme si odkázat např. na práci z roku 2017.38
Řada hypotéz - "puzzle" - epigenetické fenomény
V klasické publikaci z roku 197939 bylo dělení působení EKT rozděleno do 4 skupin: psychologické, strukturální, elektrofyziologické, biochemické. Dnes se z tohoto pohledu jeví vhodné označovat EKT za minimálně invazivní neuromodulační zákrok v armamentáriu biologické psychiatrie.
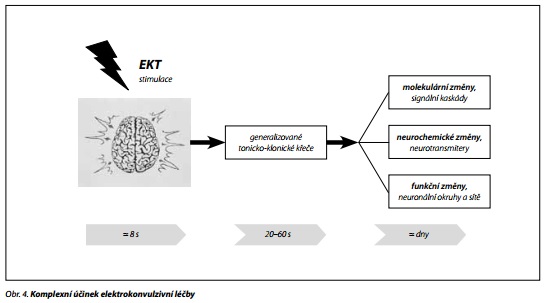
Neexistuje jednotná teorie. Lze však uvést několik hypotéz, které i ve světle počátku 21. století nadále spoluvysvětlují účinek EKT (obr. 4); z čistě didaktických důvodů jsou dělené do tří oblastí: a) molekulární změny (včetně intracelulárních signálních kaskád, změn genetické exprese, molekul akutní fáze, vlivu na buněčné membrány, neprobádaný vliv na mitochondriální funkce); b) neurochemické změny (uvažující především klasické neurotransmitery); c) funkční změny (změny na úrovni neuronů a jejich částí v neuronálních okruzích a sítích velkého dosahu).
a) psychologický mechanismus
Psychologické vysvětlení účinku vedlo ke spekulacím inspirovanými psychodynamickými konstrukty poplatnými době vzniku (50. léta - "antipsychiatric movement").40
Mezi populární psychologické teorie patřila teorie trestu, vykládaná především u pacientů s "melancholickou depresí" (výrazné pocity viny a autoakuzace, sklíčenost). Jiné teorie zvažovaly podíl amnézie samotné.41
b) "konvulzivní"
V klasické (starodávné) literatuře je možné vysledovat zmínky o výlučnosti diagnóz epilepsie a psychózy, resp. melancholie. V roce 2004 byla zpracována studie využívající SPÉCT (jednofotonová emisní tomografie) popisující význam aktivace kortiko-thalamo-kortikálních okruhů během iktální aktivity při EKT s vlivem na psychopatologii.42
c) "antikonvulzivní"
Nálezy u pacientů depresivních a katatonních z roku 2003 udávaly depleci gama-aminomáselné kyseliny (GABA) v parietálních kortikálních sítích, přičemž EKT vedla ke kompenzačnímu zvýšení funkce inhibičních neurotransmiterů (GABA) se sekundárním antidepresivním a antikonvulzivním efektem. EKT v kombinaci s NMDA agonisty (topiramát, minocyklin, amantadin, memantin) vedla ke zlepšení refrakterních organických katatonních stavů a signifikantnímu navýšení koncentrace GÁBA v okcipitální kůře, což bylo prokázáno pomocí protonové magnetické rezonanční spektroskopie.43
V animálních modelech při pokusu na bezmocných krysách bylo prokázáno zvýšení poměru glutamát/GABA v hippocampu a prefrontální kůře, po léčebném zásahu (desipramin 10 mg/kg intraperitoneálně nebo EKT) došlo k poklesu poměru glutamát/GABA v obou jmenovaných oblastech.44
d) inhibiční (gama-aminomáselná kyselina)
Efektem EKT dochází ke kompenzatornímu zvýšení GABA transmise v rámci GABA-deficientní hypotézy deprese.45
e) excitační (glutamát)
U depresivních pacientů byla46 prokázána i normalizace poměru glutamát/glutamin v levém cingulu, což může být důsledkem responze depresivních pacientů na EKT a potvrzení dalších obdobných nálezů.47
f) klasická monoaminová (ovlivnění neurotransmiterů dopaminu, serotoninu a noradrenalinu); bylo prokázáno 20% zlepšení stavu pacientů vůči tricyklickým antidepresivům a 45% zlepšení vůči inhibitorům monoaminooxidázy (MAOI) a zlepšení vůči paroxetinu.48 Rychlejší efekt oproti psychofarmakoterapeutickým přístupům byl opakovaně prokázán taktéž. 49 Tato rychlost ovšem nemusí být u všech pacientů vyjádřena ve stejné míře a EKT u pacientů po neúspěšné farmakologické léčbě má prokazatelně delší průběh k navození remise.
g) změny v transmisi acetylcholinu
Změny v transmisi acetylcholinu ve smyslu jejího snížení po EKT mohou stát v pozadí za rozvojem deliria u preexistující kognitivní poruchy.50 Souběžná léčba rivastigminem může snížit riziko rozvoje sekundárních nežádoucích účinků spojených s kognitivními funkcemi.51
h) ovlivnění endogenního opioidového systému
Byla prokázána souvislost mezi dlouhodobým užíváním opioidů a rozvojem rezistence k EKT, mechanismus není jasný.52
i) ovlivnění metabolismu tryptofan-kynurenin
Studie z roku 2016 ukázala na pozitivní vliv v neuroprotekci snížením plazmatické hladiny chinolové kyseliny u 80 % pacientů a léčba EKT byla též spojená se snížením poměru chinolát/kynurenin (patologicky zvýšený poměr u deprese vede k nadměrné aktivaci NMDA receptorů).53
j) hypothalamo-neuroendokrinní
Ve studiích z roku 198754 a 200655 byla opakovaně prokázána normalizace v dexamethazolovém supresním testu po absolvování EKT.
U těžších depresivních (zejména melancholických) stavů bývá porucha funkce osy hypothalamus-hypofýza-nadledviny.56 Opakovaně byly prokázány zvýšené hladiny kortikotropin uvolňujícího hormonu (CRH), adrenokortikotropního hormonu (ACTH) a kortizolu u depresivní poruchy. 57
k) diencefalo-neuroendokrinní
Je ovlivněn metabolismus neuropeptidu Y a substance P. Úprava poruch cyklu spánek-bdění, chuti k jídlu a libida po aplikaci EKT u depresivních pacientů vedla k úvahám o důležitosti aktivace hypothalamických funkcí (přeneseně působící neuroendokrinní změny).58
l) obecně imunitní
U depresivních pacientů byla opakovaně prokázána významná role ovlivnění imunitního systému uvnitř hematoencefalické bariéry - neuropilu.36 Změny lze pozorovat v glii, jejíž zvýšená aktivita působí neuroprotektivně.59 Nekonkluzivně jsou zmiňovány v literatuře též vlivy na lymfocyty B a mastocyty.
m) ovlivnění plazmatického epiteliálního pigmentového faktoru (PEDF)
PEDF indukuje prozánětlivé změny v mikroglii. Změny v plazmatické hladině PEDF jsou asociovány s responzí na antidepresivní léčbu. Přestože nedochází po EKT k jeho normalizaci, jsou hodnoty PEDF po výkonu zvýšeny, což naznačuje dle práce z roku 2017 možnost, že PEDF by mohla být intermediární molekulou mechanismu účinku EKT.60 Nicméně vidět mechanismus účinku v jedné molekule se zdá obskurní.
n) změny v hematoencefalické bariéře
Během konvulzivní léčby je zvýšena permeabilita bariéry. Zvýšení průchodnosti hematoencefalické bariéry je asociováno s vyšší incidencí kognitivních nežádoucích účinků. Někteří autoři naznačují, že tyto změny umožňují lepší dostupnost psychofarmak z plazmy.61
o) změny v průtoku krve mozkem
Studie prováděné metodou tomografické scintigrafie (SPECT) na populacích depresivních pacientů naznačují snížení průtoku krve ve frontálních oblastech ihned po EKT.62 Navzdory tomuto akutnímu jevu dochází posléze k relativnímu zvýšení průtoku, a tudíž k normalizaci u pacientů s poruchami depresivního spektra.63
p) změny v glukózovém metabolismu
Ve frontálním laloku, parietálním laloku a gyrus cinguli bylo po EKT pozorováno snížení regionálního glukózového metabolismu. Termín používaný pro tyto změny je "funkční postiktální suprese aktivity".64
Dále bylo prokázáno snížení glukózového metabolismu u respondérů v porovnání s nonrespondéry ve frontálních lalocích.65
Někteří autoři dokonce naznačují, že glukózový metabolismus a jeho inhibice, čili snížená energetických nároků, může výrazně přispívat k účinku EKT.64
q) neuroprotektivní vlivy
Dochází ke změnám v subklinických zánětlivých procesech v centrální nervové soustavě (vyplavovány jsou pankreatický polypeptid, C-peptid, natriuretický peptid B, interleukin 6, tumor nekrotizující faktor alfa; suprimovány jsou interleukin 8 a 13, endotelový růstový faktor, inzulínu podobný růstový faktor I, myeloperoxidáza, sortilin-1, interferon ?).66
r) neuroneogenetické vlivy
Signifikantní efekt na neuroneogenezi v lidském mozku byl prokázán v lokalizacích: hippocampus, habenula, amygdala, přední cingulum, temporální a frontální neokortex, hypothalamus. Jde o růst zprostředkovaný vyplavováním mozkového růstového faktoru (brain-derived neurotropic factor, BDNF), vaskulárního (VDNF) a gliálního růstového faktoru (GDNF) a deregulace proteinu p11.
Zásadní roli v těchto dějích hrají signální systémy, např. kaskáda cyklického adenosin monofosfátu (AMP), protein vázající responzivní částice (CREB) a jejich účinek na expresi neurotrofických faktorů, jakými je např. BDNF uplatňující se v patogenezi a léčbě depresivních poruch.
In vivo, na zvířecích modelech, byly prováděny studie, které naznačují, že antidepresivní účinky EKT mohou být připisovány vlivům terapie na neuroneogenezi a neuroplasticitu. Jedna jediná elektrokonvulze taktéž signifikantně zvyšuje koncentraci mRNA (messenger ribonukleová kyselina) pro BDNF a též tyrosin kinázu B (TrkB) mRNA, která je efektorem BDNF. Hladiny BDNF rostou nejvíce v oblasti hippocampů a v entorhinálních oblastech, přičemž BDNF mRNA a TrkB mRNA se prokazatelně zvyšují během průběhu EKT, přičemž zvýšení lokální hladiny BDNF bylo závislé na dávce (resp. přímo na počtu aplikací).
BDNF je zodpovědný za neuronální proliferaci především v gyrus dentatus a dále za větvení eferentace neuronů. VDNF zodpovídá za proliferaci cévního systému a propojení neuroneogeneze s cévním zásobením, GDNF podporuje především dopaminergní neurony.67 Dochází ke snížení globální exprese receptoru 5-HT (serotoninový receptor).68 Deregulace proteinu pil (u deprese) indukuje expresi molekul bránících deterioraci nematurované neuronální tkáně (přes 5-HT1B receptor).
s) ovlivnění dendritické arborizace
Při depresi je snížená dendritická arborizace a snížení počtu neuronů (kortex, hippocampus).
EKT jsou následovány zvýšeným formováním neuronů v hippocampů, což může být pozorováno již po jediné elektrokonvulzi, tento děj progredoval v závislosti na počtu elektrokonvulzí, tudíž lze usuzovat na závislost těchto dějů.69
Na experimentálních zvířecích modelech bylo taktéž prokázáno zvýšení protein vázající cAMP responzivní částice (CREB) a zvýšení transkripce zprostředkované právě CREB bylo objeveno v hippocampech. Chronické elektro-konvulzivní záchvaty taktéž v hippocampech pokusných myší vyvolávají rašení mechových vláken a samotné změny ve smyslu neuronálního růstu byly prokázány i v jiných částech mozku.
t) hypotézy zahrnující synaptickou plasticitu
Při dlouhodobé potenciaci (LTP) se uplatňuje redukce GABA-ergní transmise a facilituje se LTP-indukovaná tetanizace. EKT tím upravuje dysbalanci glutamát/GABA. Je ovlivněna exprese metabotropního glutamátového receptoru a některých podtypů receptoru NMDA.
Mezi bezprostřední produkty časných genů po akutní EKT patří zvýšená produkce genu Homer 1 (na více než ónásobek v neokortexu a hippocampů) a konstrukčních proteinů s možným vztahem ke vstupu Ca2+ do buňky. Dosud není vyjasněno, jakým způsobem suprese dlouhodobé deprese (LTD) navozuje antidepresivní efekt. Je pravděpodobné, že LTD není nezbytným podkladem antidepresivního účinku, ale spíše jde o kompenzační úlohu. Redukovaná excitabilita po EKT posouvá rozsah postsynaptické aktivity k upřednostnění indukce LTD. Potlačení této indukce LTD je pak schopno kompenzovat preferenci k indukci LTD.70
u) změny ve funkční konektivitě frontálního a temporálního kortexu
Zvýšená regionální mozková aktivita byla zjištěna pomocí metody magnetickou rezonancí měřené nízkofrekvenční fluktuace (ALFF) hlavně v levém subgenikulárním anteriorním cingulu (sgACC) po EKT. Funkční spojitost sgACC se zvýšila v ipsilaterálním parahippokampálním gyru, pregenikulárním anteriorním cingulu, kontralaterálním středním temporálním gyru a orbitofrontálním kortexu. Byla prokázána asociace mezi ústupem depresivních příznaků a funkční konektivitou sgACC.71
v) změny v kortiko-subkortikálnífunkční konektivitě
Časné změny v poklesu intralimbické funkční konektivity (měřeno pomocí magnetické rezonance) signifikantně predikují pozdější zvýšení v limbicko-prefrontální konektivitě, což ve výsledku signifikantně predikuje klinické zlepšení na konci série EKT.72
w) neurofyziologické změny
Elektrokonvulze mají svůj typický korelát při měření elektroencefalogramem (EEG). Tato oblast zasluhuje samostatnou publikaci. Významnými indikátory efektivity EKT jsou tzv. index postiktální suprese (postictal suppression index, PSI) a index suprese výbojové aktivity (burst suppression index, BS). Jejich změny souvisejí se změnami konvulzivního prahu a souvisejí s antidepresivním účinkem.73 Klinický význam je však zřejmě minimální.
x) retikulo-thalamo-mezencefalické změny
Během EKT je pozorováno zvýšení aktivity v oblasti retikulární formace mozkového kmene, bazálních ganglií, mezencefala, amygdaly, thalamu a hypothalamu, následované snížením aktivity EEG v těchto oblastech. Pouze v thalamu zůstala vyšší aktivace než před terapií, která korelovala s pomalou rytmickou aktivitou EEG propagovanou do neokortexu.74
y) hypotézy o aktivaci genů akutní fáze
Jsou popsány signifikantní změny v plazmatické koncentraci látek: CD40L, interleukiny 8 a 13,endoteliální růstový faktor (EGF), insulinu podobný růstový faktor-1 (IGF-1), myeloperoxidáza, sortilin-1, interferon-?, pankreatický polypeptid, C-peptid, mozkový natriuretickýpeptid, lipopoly-sacharidem stimulovaný interleukin 6, tumor nekrotizující faktor ?, faktor kmenových buněk (SCF). Dosud nekonkluzivní jsou změny apolipoproteinu E.75
z) aktivace genů přímo reagujících na průchod elektrického proudu buňkou
Bienenstockova-Cooperova-Munroova teorie popisuje změny v CNS na principu aktivace genu Homer 1 s výsledným vlivem na antiapoptotické děje přes regulaci intracelulárního metabolismu vápníku. Gen Homer 1 obsahuje doménu vážící se na specifické receptory v buněčné membráně a "coiled-coil" (CC) domény vážící se navzájem (dimerizace). Jsou dvě varianty: Homer 1b/c (konstituční) a Homer 1a (závislá na aktivaci). mRNA genu Homer 1b/c obsahuje všechny exony kódující CC doménu, zatímco mRNA Homer 1a nenese exony CC domény, ale obsahuje krátký řetězec kódující 11aminokyselinový segment. Homer 1a bez CC domény může působit jako dominantně negativní blokátor Homer 1b/c. Mezi receptory s prolinem bohatou sekvencí vážící tuto doménu patří metabotropní glutamátový receptor (mGluR) a inositol-1,4, 5-trifosfátový receptor (IP3R) a adaptační proteiny (např. Shark).
Dimerizace konstitučně přítomné Homer 1b/c obsazuje receptor (včetně mGluR skupiny 1 a IP3R). Aktivitou indukovaná expresivita Homer 1a narušuje kotvení konstituční varianty přes CC doménu. Teoretický model fenomenologie synaptické plasticity zdůrazňuje polaritu změn synaptické aktivity a je regulována podle počtu post-synapticky aktivovaných neuronů, což je ekvivalentem elevace postsynaptického Ca2+ po aktivaci synapse. Předpokládá se, že nevelký nárůst Ca2+ vede k LTD, větší elevace pak k LTR Je možno vytvořit bifázickou křivku vztahu vstupu/výstupu. A teorie ukazuje, že facilitace Ca2+ kanálků vlivem Homer 1a posouvá disociativní křivku koncentrace intracelulárního vápníku doleva, a tím vede k potlačení neuronální apoptózy při elektrokonvulzivní léčbě depresivního syndromu. 76
Vliv genetického polymorfismu a (do budoucna) epigenetických faktorů
Je důležité zdůraznit, že genetický polymorfismus hraje velmi důležitou roli v účinku EKT podobně jako při psychofarmakologické léčbě. Známe rozdílný vliv EKT na psychopatologii při polymorfismu genu pro katechol-o-methyltransferázu (COMT, Val158Met), kdy alela Val má vyšší enzymatickou aktivitu než Met, a u homozygotů Met/Met byla zaznamenána vyšší koncentrace dopaminu v prefrontální šedé kůře po elektrokonvulzích.
Zajímavý je též gen pro dopaminový receptor 2 (DRD2J, kdy byl pozorován výraznější efekt EKT u CC genotypu DRD2 (C957T) v kombinaci s Val/Val COMT.77
ZÁVĚR
Elektrokonvulzivní léčba je v klinické praxi nepostradatelnou a nenahraditelnou, rychlou, účinnou, bezpečnou a dobře snášenou metodou. Patří mezi běžné léčebné postupy s prokazatelnou účinností. Má omezené indikační spektrum. V ČR se aplikuje u cca 1000 pacientů ročně.78 Celá řada nových modifikací je ve stadiu intenzivního výzkumu a klinických zkoušek.
EKT se aplikují v lůžkovém psychiatrickém zdravotnickém zařízení se zavedeným anesteziologickým pracovištěm u hospitalizovaných nebo ambulantních pacientů. Pořízení přístrojů je velmi nákladné, návratnost nepřiměřená. Provoz je materiálně méně náročný. O to cennější je fungující zaběhnutý elektrokonvulzivní tým. Za narkózu je zodpovědný anesteziolog. Za celý průběh výkonu EKT je zodpovědný vyškolený psychiatr specialista.
Samotný výkon EKT je hrazen z prostředků veřejného zdravotního pojištění (kód 35710) a ohodnocen jen 362 body při časové dotaci 30 minut (viz Číselník zdravotních výkonů 1147 platný od 1. 1. 2017 na stránkách www.vzp.cz); v nákladech nutno počítat i s celkovou anestezií. Výkony v experimentálních modifikacích (MST jako konvulzivní varianta rTMS a FEAST jako konvulzivní varianta tDCS) nejsou bohužel dosud hrazeny ze všeobecného zdravotního pojištění.
Platí stále ještě paradigma: Bez motorického projevu tonicko-klonických křečí (na což má vliv nejen dávka energie, dávka anestetika, užívání benzodiazepinů, antiepileptik a jiných léků a hloubka myorelaxace), jsou elektrokonvulze abortivní a klinicky neúčinkují? Vyplatí se sledovat jednokanálové EEG obou hemisfér a označit paroxysmus kratší než 20 s za abortivní?
Povede výzkum FEAST a MST, rTMS a tDCS a dalších biologických modalit ve spojení s nejmodernějšími poznatky nejen neurozobrazovacích disciplín k hledané "sjednocené teorii mechanismu účinku elektromagnetismu na psychopatologii člověka"?
LITERATURA
- 1. Coffey CE. The Clinical Science of Electroconvulsive Therapy. APA 1993: 282.
- 2. Černoušek M: Studie k dějinám psychiatrického myšlení II. Praha: Novinář 1988.
- 3. Mádlová K, Kališová L, Albrecht J et al. Historický přehled vývoje elektrokonvulzivní terapie. Čes a slov Psychiat 2015; 111 (6): 306-313.
- 4. Lisanby SH, Schlaepfer TE, Fisch HU et al. Magnetic seizure therapy of major depression. Arch Gen Psy 2001; 58 (3): 303-305.
- 5. Sackeim HA. Convulsant and anticonvulsant properties of electroconvulsive therapy: toward a focal form of brain stimulation. Clin Neurosci Res 2004; 4: 39-57.
- 6. Spellman T, Peterchev AV, Lisanby SH. Focal Electrically Administered Seizure Therapy (FEAST): A novel form of ECT illustrates the roles of current directionality, polarity, and electrode configuration in seizure induction. Neuropsychopharmacol 2009; 34 (8): 2002-2010.
- 7. Tufail Y, Matyushov A, Baldwin N et al. Transcranial pulsed ultrasound stimulates intact brain circuits. Neuron 2010; 66 (5): 681-694.
- 8. Kayser S, Bewernick BH, Grubert C et al. Antidepressant effects of magnetic seizure therapy and electroconvulsive therapy, in treatment-resistant depression. J psychiatr res 2011; 45 (5): 569-576.
- 9. Baghai TC, Möller HJ. Electroconvulsive therapy and its different indications. Dialogues Clin Neurosci 2008; 10 (1): 105-117.
- 10. Dierckx B, Heijnen WT, van den Broek WW et al. Efficacy of electroconvulsive therapy in bipolar versus unipolar major depression: a meta-analysis. Bipolar Disord 2012; 14: 146-150.
- 11. Caravalho AE Vieta E. The treatment of bipolar disorder. Integrative Clinical strategies & future directions. Oxford University Press 2017: 410-422.
- 12. Wenzheng W, Chengcheng P, Jiangling J et al. Efficacy and safety of treating patients with refractory schizophrenia with antipsychotic medication and adjunctive electroconvulsive therapy: a systematic review and meta-analysis. Shanghai Arch Psychiatry 2015; 27 (4): 206-219.
- 13. Mashimo K, Sato Y, Yamauchi T. Effective electroconvulsive therapy for stupor in the high risk patient: a report of two cases. Psychiatry Clin Neurosci 1996; 50 (3): 129-131.
- 14. Federica L, Pierpaolo M, Michela CM et al. Electroconvulsive therapy in catatonic patients: Efficacy and predictors of response. World J Psychiatry 2015; 5 (2): 182-192.
- 15. Fink M. Katatonie: často se vyskytující klinický syndrom, rozpoznatelný a léčitelný. Čes a slov Psychiat 2017; 113 (2): 84-93.
- 16. Lee BS, Huang SS et al. Clinical features of delirious mania: a series of five cases and a brief literature review. BMC Psychiatry 2012; 12: 65.
- 17. Karmacharya R, England ML, Ongiir D. Delirious mania: Clinical features and treatment response. Journal of Aff Dis 2008; 109 (3): 312-316.
- 18. Kellner CH, Fink M, Knapp R et al. Relief of Expressed Suicidal Intent by ECT: A Consortium for Research in ECT Study. Am J Psychiatry 2005; 162 (5): 977-982.
- 19. Ujkaj M, Davidoff DA, Seiner SJ et al. Safety and efficacy of electroconvulsive therapy for the treatment of agitation and aggression in patients with dementia. Am J Geriatr Psychiatry 2012; 20 (1): 61-72.
- 20. Vizcainoa EJV, Sanza DB, Fuentenebrob JS. Electroconvulsive therapy as treatment for malignant neuroleptic syndrome. Rev Psiquiatr Salud Ment 2011; 4: 169-176.
- 21. Zeiler FA, Matuszczak M, Teitelbaum J et al. Electroconvulsive therapy for refractory status epilepticus: A systematic review. Seizure Eur J Epilep 2016; 35: 23-32.
- 22. Lambrecq V, Villéga F, Marchal C et al. Refractory status epilepticus: Electroconvulsive therapy as a possible therapeutic strategy. Seizure 2012; 21 (9): 661-664.
- 23. Andersen K, Balldin J, Gottfries CG et al. A double-blind evaluation of electroconvulsive therapy in Parkinson´s disease with "on-off" phenomena. Acta Neurol Scand 1987; 76 (3): 191-199.
- 24. Furukori NY, Kikuchi A, Katagai H. The effects of electroconvulsive therapy on tardive dystonia or dyskinesia induced by psychotropic medication: a retrospective study. Neuropsychiatr Dis Treat 2014; 10: 1209-1212.
- 25. Nielsen RM, Olsen KS, Lauritsen AO. Electroconvulsive therapy as a treatment for protracted refractory delirium in the intensive care unit - five cases and a review. J Crit Care 2014; 29 (5).
- 26. Procopio M. NICE guidelines and maintenance ECT. Brit J Psychiat 2003; 183 (3): 263.
- 27. Petrides G, Tobias KG, Kellner CH et al. Continuation and Maintenance Electroconvulsive Therapy for Mood Disorders: Review of the Literature. Neuropsychobiology 2011; 64 (3): 129-140.
- 28. Youssef NA, McCall WV, Andrade C. The role of ECT in posttraumatic stress disorder: A systematic review. Ann Clin Psy 2017; 29 (1): 67-70.
- 29. Hosák L. Novinky v elektrokonvulzivní terapii. Psychiat pro praxi 2010; 11 (1): 22-24.
- 30. Nemeroff CB ed. Management of Treatment-Resistant major psychiatrie disorders. Oxford University Press 2012: 400.
- 31. Torring N, Sanghani SN, Petrides G. The mortality rate of electroconvulsive therapy: a systematic review and pooled analysis. Acta Psychiatr Scand 2017; 135: 388-397.
- 32. Kubinová M, Michalec J, Kališová L et al. Elektrokonvulzivni terapie a její vliv na kognitivní funkce. Psychiatrie 2017; 21 (suppl. 2): 10-11.
- 33. Mádlová K, Kališová L, Albrecht J et al. Stigma spojené s elektrokonvulzivni terapií (EKT). Psychiatrie 2017; 21 (suppl. 2): 10-11.
- 34. Köhler R. Elektrokonvulzivni terapie. Psychiatr pro praxi 2014; 15 (1).
- 35. Mankad MV, Beyer JL, Weiner RD et al. Clinical Manual of Electroconvulsive Therapy. APA 2010: 239.
- 36. Sartorius N, Holt RIG, Maj M (eds): Comorbidity of Mental and Physical Disorders. Key issues Ment Health. Basel: Karger2015; 179: 99-112.
- 37. ONeill-Kerr A, Yassin A, Rogers S et al. Switching From Age-Based Stimulus Dosing to Dose Titration Protocols in Electroconvulsive Therapy: Empirical Evidence for Better Patient Outcomes With Lower Peak and Cumulative Energy Doses. J ECT 2017; 33 (3): 181-184.
- 38. Weiner RD, Reti IM. Key updates in the clinical application of electroconvulsive therapy. Brain Stim 2017; 29: 54-62.
- 39. Fink M. Convulsive therapy: Theory and Practice. New York: Raven Press 1979.
- 40. Bolwig T. How does electroconvulsive therapy work? Theories on its mechanism. Can J Psychiat 2011; 56 (1): 13-18.
- 41. Ottoson J. Experimental studies of the mode of action of electroconvulsive therapy: Introduction. Acta Psychiatr Scand 1960; 35 (145): 5-6.
- 42. McNally K, Blumenfeld H. Focal network involvement in generalized seizures: new insights from electroconvulsive therapy. Epilepsy Behav 2004; 5(1): 3-12.
- 43. Sanacora, G, Mason GF, Rothman DL et al. Increased cortical GABA concentrations in depressed patients receiving ECT. Am J Psychiatr 2003; 160: 577-579.
- 44. Sartorius A, Mahlstedt MM, Vollmayr B et al. Elevated spectroscopic glutamate/gamma-amino butyric acid in rats bred for learned helplessness. NeuroReport 2007; 18: 1469-1473.
- 45. Sackeim HA. Review The anticonvulsant hypothesis of the mechanisms of action of ECT: current status. J ECT 1999; 15(1): 5-26.
- 46. Palmio J, Huuhka M, Saransaari P et al. Changes in plasma amino acids after electroconvulsive therapy of depressed patients. Psychiatry Res 2005; 137(3): 183-190.
- 47. Pfleiderer B, Michael N, Erfurth A et al. Effective electroconvulsive therapy reverses glutamate/glutamine deficit in the left anterior cingulum of unipolar depressed patients. Psychiatry Res 2003; 122 (3): 185-192.
- 48. Janicak PG, Davis JM, Gibbons RD et al. Efficacy of ECT: a meta-analysis. Am J Psychiatr 1985; 142 (3): 297-302.
- 49. Sackeim HA, Decina P, Kanzler M et al. Effects of electrode placement on the efficacy of titrated, low-dose ECT. Am J Psychiatry 1987; 144: 1449-1155.
- 50. Pigot M, Andrade C, Loo C. Pharmacologial attenuation of electroconvulsive therapy-induced cognitive deficits: theoretical background and clinical findings. J ECT 2008; 24 (1): 57-67.
- 51. Van Shaick AM, Rhebergen D, Henstra MJ. Cognitive impairment and Elecetroconvlusive therapy in geriatric depression, What Could bet he Role of Rivastigmine? A case Series. Clin Pract 2015; 5 (3): 780.
- 52. Scherrer JF, Salas J, Sullivan MD et al. The influence of prescription opioid use duration and Dose on Developement of Treatmenr Resistant Depression. Prev Med 2016; 91: 110-116.
- 53. Schwieler L, Samuelsson M, Frye MA et al. Electroconvulsive thrapy suppresses the neurotoxic branch of the kynurenine pathway in treatmen-resistant depressed patients. J Neuroinflammation 2016; 13: 51.
- 54. Grunhaus L, Zelnik T, Albala AA et al. Serial dexamethasone suppression tests in depressed patients treated only with electroconvulsive therapy. J Affect Disord 1987; 13 (3): 233-240.
- 55. Kunugi H, Ida I, Owashi T et al. Assessment of the dexamethasone/CRH test as a state-dependent marker for hypothalamic-pituitary-adrenal (HPA) axis abnormalities in major depressive episode: a multicenter study. Neuropsychopharmacol 2006; 31: 212-220.
- 56. Sapolsky R. Glucocorticoids and hippocampal atrophy in neuropsychiatric disorders. Arch Gen Psychiatr 2000; 57 (10): 925-935.
- 57. Holsboer F. Review The corticosteroid receptor hypothesis of depression. Neuropsychopharmacol 2000; 23 (5): 477-501.
- 58. Fink M, Ottosson J. A theory of convulsive therapy in endogenous depression: significance of hypothalamic functions. Psychiatr Res 1980; 2 (1) : 49-61.
- 59. Van Buel EM, Pattas K, Peters M et al. Immune and neurotrophin stimulation by electroconvulsive therapy: is some inflammation needed after all? Transl Psychiatr 2015; 5 (7): e609.
- 60. Ryan KM, Glaviano A, O´Donovan SM et al. Electroconvulsive therapy modulates plasma pigment epithelium-derived factor in depression: a proteomics study. Transl Psychiatr 2017; 7 (3): e1073.
- 61. Ito M, Bolati K, Kinjo T et al. Electroconvulsive stimulation transiently enhances the permeability of the rat blood-brain barrier and induces asctrocytic changes. Brain Res Bull 2017; 128: 92-97.
- 62. Scott Al, Dougall N, Ross M et al. Short-term effects of electroconvulsive treatment on the uptake of 99mTc-exametazime into brain in major depression shown with single photon emission tomography. J Affect Disord 1994; 30: 27-34.
- 63. Bonne O, Krausz Y, Shapira B et al. Increased cerebral blood flow in depressed patients responding to electroconvulsive therapy. J Nucl Med 1996; 37 (7): 1075-1080.
- 64. Nobler MS, Oquendo MA, Kegeles LS et al. Decreased regional brain metabolism after ECT Am J Psychiatr 2001; 158 (2): 305-308.
- 65. Nobler MS, Teneback CC, Nahas Z et al. Structural and functional neuroimaging of electroconvulsive therapy and transcranial magnetic stimulation. Depress Anxiety 2000; 12 (3): 144-156.
- 66. Altar CA, Laeng P, Jurata LW et al. Electroconvulsive seizures regulate gene expression of distinct neurotrophic signaling pathways. J Neurosci 2004; 24: 2667-2677.
- 67. Chen AC, Shin KH, Duman RS et al. ECS-Induced mossy fiber sprouting and BDNF expression are attenuated by ketamine pretreatment. J ECT 2001; 17: 27-32.
- 68. Svenningsson P, Chergui K, Rachleff I et al. Alterations in 5-HT1B receptor function by pi 1 in depression-like states. Science 2006; 311, 77-80.
- 69. Newton SS, Girgenti MJ, Collier EF et al. Electroconvulsive seizure increases adult hippocampal angiogenesis in rats. Eur J Neurosci 2006; 24: 819-828.
- 70. Kato N. Neurophysiological mechanisms of electroconvulsive therapy for depression. Review article. Neurosci Res 2009; 64: 3-11.
- 71. Liu Y, Du L, Li Y et al. Antidepressant Effects of Electroconvulsive Therapy correlate with subgeniual anterior cingulate aktivity and connectivity in depression. Baltimore: Medicine 2015; 94 (45): e2033.
- 72. Cano M, Cardoner N, Urretavizcaya M et al. Modulation of Limbic and Prefrontal Connectivity by Electroconvulsive Therapy in Treatment-resistant Depression: A Preliminary Study. Brain Stimulation 9; 2016: 65-71.
- 73. Singh A, Kar SK. How Electroconvulsive Therapy Works?: Understanding the Neurobiological Mechanisms. Clin Psychopharmacol Neurosci 2017; 15 (3): 210-221.
- 74. Fosse R, Read J. Electroconvulsive treatment: hypothesis about Mechanism of Action. Front Psychiatr 2013; 4: 94.
- 75. Stelzhammer V, Guest PC, Rothermundt M et al. Electroconvulsive therapy exerts mainly acute molecular changes in serum of major depressive disorder patients. Eur Neuropsychopharmacology 2013; 23: 1199-1207.
- 76. Dunlop BW, Nemeroff CB. The role of dopamine in the pathophysiology of depression. Arch Gen Psychiatry 2007; 64: 327-337.
- 77. Conti B, Maier R, Barr AM et al. Region-specific transcriptional changes following the three antidepressant treatments electroconvulsive therapy, sleep deprivation and fluoxetine. Mol Psychiatry 2007; 12: 167-189
- 78. Kalisova L, Madlova K, Albrecht J, Michalec J, Kubinova M. Use of electroconvulsive therapy in the Czech Republic. J of ECT 2017 in press.





